Применение PRP в лечении акне: механизмы действия и результаты
Какое место в терапии акне отводится плазмотерапии? На какие звенья патогенеза угревой болезни направлено воздействие PRP? Какими факторами обусловлено положительное влияние PRP на репаративные процессы в коже? В чем особенности такого класса препаратов обогащенной тромбоцитами плазмы крови, как P-PRP?
Одна из сложнейших загадок в дерматологии и косметологии – лечение акне, поскольку этиология этого заболевания до сих пор не ясна. Почему у кого-то возникает акнеформный дерматоз, а у кого-то нет?
Известно много факторов, предрасполагающих к его возникновению. Самый главный из них — это отягощенная по акне наследственность. Также существует много механизмов, запускающих процесс заболевания при наличии наследственного фактора. Например, одним из важнейших триггеров служит стресс, так как на его фоне возникает дисбаланс на гормональном уровне, что является одним из звеньев патогенеза угревой болезни.
Механизмы развития акне изучены довольно широко, поэтому в дерматологии и косметологии с успехом применяется патогенетическое лечение, а не этиотропное. Зная четко звенья патогенеза, мы можем влиять на них разными методами лечения. При этом мы обязаны руководствоваться в каждом конкретном случае постановкой правильного диагноза, а именно определением формы акне, степени тяжести, стадии и течения процесса (хроническое или острое) — от этого зависит выбор методики лечения и успех последнего.
Сегодня принято выделять следующие основные звенья патогенеза акне:
1) гиперпродукция кожного сала под воздействием мужских половых гормонов при гиперандрогении;
2) гиперпродукция кожного сала концевыми отделами сальных желез при повышенной чувствительности себоцитов к нормальному уровню в крови андрогенов;
3) генетически обусловленное высокое значение фермента 5-альфа-редуктазы, который переводит неактивный тестостерон в его активный метаболит ДГТ (дигидротестостерон);
4) гиперкератоз в области пор, приводящий к закупорке последних и нарушению отхождения сала из протоков;
5) толстая пористая кожа – слишком длинные и извитые протоки сальных желез;
6) наличие гноеродной флоры в протоках сальных желез;
7) воспаление: усиление жизнедеятельности гноеродной флоры в протоках (размножение) приводит к реагированию местного иммунного надзора кожи и появлению воспалительного процесса.
Как можно повлиять на все эти звенья патогенеза?
Во-первых, принимаем меры для уменьшения секреции кожного сала. Действуем в двух направлениях: совместно с гинекологом-эндокринологом проводим диагностику и коррекцию гормонального профиля, а также уже своими силами – фототерапию, например с применением ELOS в диапазоне длин волн 520-650 нм. Таким образом, получаем подсушивающий эффект.
Во-вторых, обеспечиваем кератолитическое воздействие (нам нужно очистить поры); для этого подходит все та же фототерапия, курс поверхностных и поверхностно-срединных пилингов с 30% салициловой кислотой, и, безусловно, обязателен правильно подобранный домашний уход за кожей.
В-третьих, проводим антибактериальное и противовоспалительное лечение с помощью фототерапии либо салициловых пилингов.
В-четвертых, мы должны убрать дополнительные предпосылки к воспалению, а именно – сократить длину протока сальной железы. Для этого мы прибегаем к лазерной шлифовке кожи. С ее же помощью запускаем процессы репарации, обновления кожи, корректируя рубцы и пятна посткне (как минимум — уменьшая их выраженность). Однако лазерную шлифовку мы можем применить только после удаления всех активных воспалительных очагов. Для этой цели и для усиления заживления кожи применяем плазмотерапию.
Надо сказать, что сегодня методы воздействия на воспалительные и репаративные процессы при акне и постакне активно обсуждаются на профессиональных встречах косметологов и дерматологов. Особое внимание в этом плане привлекает плазмотерапия — применение PRP, то есть аутологичной плазмы крови, обогащенной тромбоцитами (Platelet Rich Rlasma).
Антибактериальное и противовоспалительное действие плазматерапии на акне
Многие авторы обращают внимание на то, что в развитии и /или поддержании воспалительного процесса в сально-волосяных фолликулах и на поверхности кожи не последнюю роль могут играть не только пропионибактерии, но и стафилококки и грибы Malassesia.
Исследования микробного пейзажа кожи, пораженной различными формами акне, показали, что практически у 90% пациентов обнаруживали увеличение численности стафилококков, как золотистого, так и эпидермального, примерно у 65% отмечалось значительное увеличение количества стрептококков, причем на фоне существенного роста численности коринебактерий ( Е.Ф. Колмакова, О.С Панова и соавт., 2010). Большинство выделенных штаммов устойчивы к действию антибиотиков и антимикробной химиотерапии при акне (Г.Н. Бурцева и соавт., 2013).
Установлено, что PRР демонстрирует бактериостатический потенциал в отношении метициллин-резистентных штаммов St. Aureus и St. Epidermidis за счет повышения защитных свойств кожи посредством воздействия на механизмы местного иммунного надзора (Эдуардо Анитуа, 2011-2015). Однако следует отметить, что механизм антибактериального действия PRP еще до конца не ясен. Предполагают, что он связан с содержащимися в тромбоцитах антимикробными пептидами. К настоящему времени выделено 7 таких пептидов: fibrinopeptide A, fibrinopeptide B, thymosin b-4, platelet basic protein, connective tissue activating peptide 3, RANTES, platelet factor 4.
Роль хемиконов в механизме иммунного ответа кожи
Рассмотрим механизм иммунного ответа кожи, вызванного воздействием PRP. Из тромбоцитов PRP при их активации высвобождаются хемотаксические цитокины, или хемокины (цитокины — небольшие пептидные информационные молекулы), которые участвуют в развитии иммунного ответа:
- CXCL7 (NAP-2) — (пептид, активирующий нейтрофилы-2) оказывает влияние на миграцию и активацию нейтрофилов.
- RANTES (CCL5) — хемокин, выделяемый T-клетками при их активации, задерживает сигналы моноцитов и активирует Т-клетки, эозинофилы, базофилы, натуральные киллеры и дендритные клетки.
- PF4(CXCL4) — тромбоцитарный фактор 4 (PF4), относящийся к хемокинам из семейства СХС-цитокинов, принимает участие в аттракции моноцитов и индуцирует среди рекрутированных мононуклеарных фагоцитов функциональный фенотип макрофагов с противовоспалительными и репаративными функциями.
По данным Bendinelli и соавт. (2010), при противовоспалительном эффекте PRP наблюдается редукция экспрессии генов COX2 и CXCR4, участвующих в реакциях воспаления.
Бактериостатический эффект возникает за счет повышения защитных свойств кожи через воздействие на механизмы местного иммунного надзора. Иными словами, мы провоцируем воспаление, вызываем иммунный ответ, чтобы в итоге прекратить воспалительный процесс и получить бактериостатический эффект.
Классы PRP
По классификации PAW, все препараты PRP подразделяются на 4 класса в зависимости от наличия в них лейкоцитов и фибрина:
- P-PRP (Pure Platelet Rich Plasma) – чистая (без лейкоцитов) обогащенная тромбоцитами плазма крови;
- L-PRP (Leucocyteand Platelet Rich Plasma) – обогащенная лейкоцитами и тромбоцитами плазма крови;
- P-PRF (Pure Platelet Rich Fibrin) – чистый обогащенный тромбоцитами фибрин;
- L-PRF (Leucocyteand Platelet Rich Fibrin) – обогащенный лейкоцитами и тромбоцитами фибрин.P-PRP( Pure Platelet Rich Plasma) [1].
[1] Более подробно см.: Е. Федякова. Плазмотерапия: эндогенный подход к регенерации кожи//Ki. — 2014. — № 2. — С.
PRP как фактор, активизирующий заживление кожи
Известно, что репарации (заживлению) поврежденной ткани предшествуют процессы апоптоза/некроза резидентных клеток и последующее за ними воспаление. Зная механизмы влияния PRP на воспаление, становится ясно, почему ее воздействие на поврежденную кожу приводит к значительному усилению репаративных процессов.
Механизм репарации при использовании PRР заключается в следующем.
На первом этапе происходит дегрануляция активированных ионами кальция тромбоцитов, которая приводит к их экзоцитозу и высвобождению биологически активных факторов роста и цитокинов. Согласно данным ряда авторов, высвобождение основного количества факторов роста и цитокинов происходит в течение часа.
На втором этапе происходит формирование фибриновых сгустков, которые затем превратятся в фибриновую сеть (каркас), последняя будет поддерживать объем в области введения препарата. Тромбоциты, встроившись в фибриновую сеть (геля, матрикса), продолжат секретировать биоактивные агенты на протяжении не менее 7 дней.
Факторы роста PRP взаимодействуют с поверхностными рецепторами клеток-мишеней. Показано, что на ММСК (мультипотентных мезенхимальных стромальных клетках), остеобластах, фибробластах, эндотелиальных и эпидермальных клетках имеются специфические для факторов роста PRP рецепторы. При этом они активируют внтуриклеточные сигнальные пути, индуцирующие механизмы репарации ткани, в основе которых – пролиферация и дифференциация клеток, синтез компонентов МКМ. Ключевую роль в данных процессах играют такие факторы, как PDGF (фактор роста тромбоцитов), TGF (трансформирующий ростовый фактор), IGF (инсулиноподобный фактор роста), EGF (эпидермальный фактор роста). В регуляции хемотаксиса и миграции клеток активно участвуют также содержащиеся в PRP адгезивные белки: фибрин, фибронектин, тромбоспондин и др. (Зорин В.Л., Зорина А.И., 2014).
Итак, мы рассмотрели действие PRР на таком этапе патогенеза акне, как воспаление, и на репарацию кожи после разрешения воспалительных элементов или после применения инвазивных методов коррекции постакне. Далее представим несколько клинических случаев, подтверждающих эффективность применения PRР при акне разной степени тяжести.
Клинический опыт
В практике нашей клиники мы используем технологию ENDORET PRGF — эндогенную регенеративную технологию применения плазмы крови, обогащенной факторами роста (Endogenous Regenerative Technology Plasma Rich of Growth Factors). PRGF является представителем класса P-PRP по классификации PAW. В отличие от других классов здесь полностью отсутствуют лейкоциты в конечном продукте (тромбоцитарном концентрате). Применение P-PRP характеризуется более длительной и более интенсивной продукцией факторов роста по сравнению с L-PRP (Эдуардо Анитуа, 2011-2015).
Результаты исследований также подтверждают вывод о большем регенеративном эффекте при использовании именно P-PRP, в частности PRGF. Последняя отличается от других плазмотехнологий оптимальной концентрацией тромбоцитов в единице объема плазмы — в 2,5 раза выше, чем в ОЦК (объем циркулирующей крови). В исследованиях Эдуардо Анитуа, автора технологии, было показано, что именно при такой концентрации максимально проявляются регенеративные свойства обогащенной тромбоцитами аутологичной плазмы. Введение PRGF вызывало усиленную выработку фибробластами двух особенно важных компонентов для регенерации тканей — гиалуроновой кислоты и фактора роста гепатоцитов (HGF). Последний является мощным противофиброзным агентом.
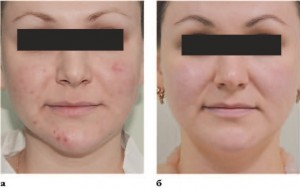
Фото 1. Пациентка Н., 30 лет, с папулопустулезной формой акне легкой степени: а — до, б — после проведения комплексного лечения, включающего плазмотерапию ENDORET PRGF.
Клинический пример 1
Пациентка Н., 30 лет. Диагноз: папулопустулезная форма акне легкой степени, подострой стадии, хронического течения; постакне — атрофические рубцы.
Лечение поэтапное:
1. Для купирования очагов воспаления были выполнены: 1 процедура салицилового пилинга (30%) и через 10 дней 1-я процедура плазмотерапии ENDORET PRGF.
2. Через 3 недели после процедуры плазмотерапии была проведена лазерная шлифовка на СО2-лазере.
Результаты первых двух этапов: достигнуто полное купирование всех воспалительных элементов.
3. Спустя 2 недели после лазеротерапии был продолжен курс ENDORET PRGF — проведены 2-я и 3-я процедуры с интервалом между ними в 3 недели.
Результаты лечения: кожа лица полностью очистилась — устранены очаги воспаления, минимизированы атрофические рубцы постакне (фото 1).
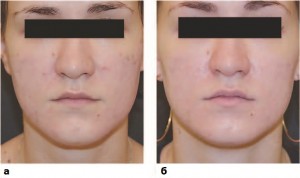
Фото 2. Пациентка А., 18 лет с папулопустулезной формой акне: а — до, б — после комбинированного лечения, включающего плазмотерапию ENDORET PRGF.
Клинический пример 2
Пациентка К., 18 лет. Диагноз: папулопустулезная форма акне средней степени тяжести, острой стадии, хронического течения; атрофические рубцы постакне.
Результаты лабораторно-инструментального исследования показали нарушение гормонального профиля — наличие гиперандрогении. По назначению гинеколога-эндокринолога пациентка начала принимать ОК с целью коррекции гормонального дисбаланса.
Была поэтапно проведена комбинированная терапия:
1. плазмотерапия ENDORET PRGF – 2 процедуры с интервалом в 3 недели;
2. через 3 недели — 1 процедура лазерной шлифовки лица (СО2-лазер);
3. через 3 недели — 3-я процедура PRGF.
Результат: достигнута ремиссия акне, выраженность рубцов постакне минимизирована (фото 2).
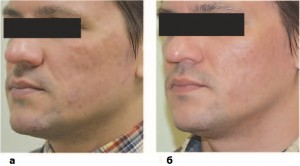
Фото 3. Пациент А., 40 лет с хроническим вялотекущим акне папулопустулезной формы: а — до, б — после 3 процедур ENDORET PRGF.
Клинический пример 3
Пациент А., 40 лет. Диагноз: вялотекущее акне папулезной формы, легкой степени, хронического течения; постакне — атрофические рубцы и застойные пятна.
Лечение: курс из 3 процедур ENDORET PRGF (фото 3), лазеротерапия с применением СО2-лазера.
Результат: были устранены воспалительные элементы акне, уменьшена выраженность рубцовых изменений кожи.
Выводы
Клиническая практика нашей клиники подтверждает эффективность применения ENDORET PRGF с целью лечения папулопустулезной формы акне легкой и средней степени тяжести и коррекции постакне — атрофических рубцов и застойных пятен. Использование этой технологии как в составе комбинированной программы лечения акне и постакне, так и в качестве монотерапевтического метода патогенетически оправдано.
Автор статьи: Яна Горяева, врач-дерматолог, косметолог клиники Beauty Trend, Москва
* По материалам доклада, представленного компанией «Доктор Тренд» на XIV Международном конгрессе по эстетической медицине (февраль 2015, Москва).